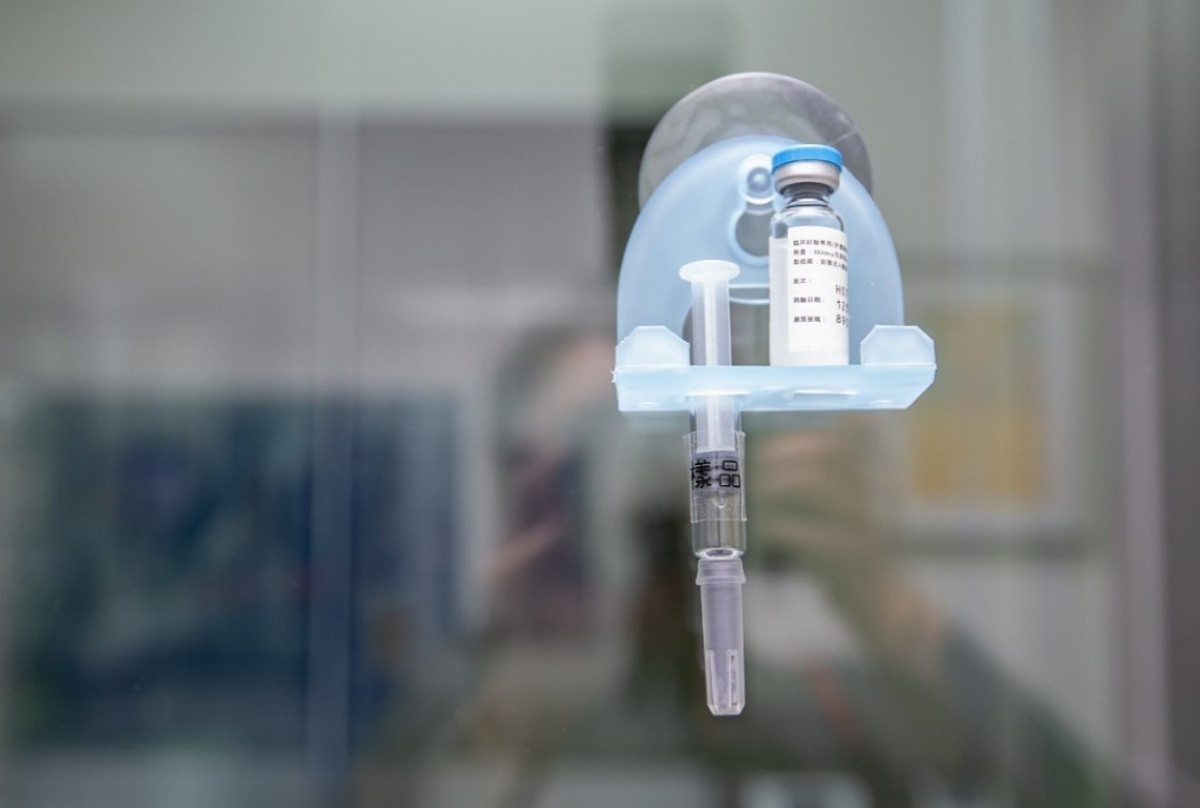
衛福部25日宣布,已通過聯亞生技的武漢肺炎疫苗臨床試驗計劃,即起可施打受試者,讓台灣研發自有武肺疫苗的進度上,再向前跨出一步。(資料照,圖/總統府Flickr)
從中國湖北武漢爆發的武漢肺炎(或稱COVID-19、新冠肺炎),這8個月多已成全球流行性傳染病。目前包含美國、英國、德國、中國等世界多國除持續防範武肺疫情進一步肆虐外,也積極研發武肺疫苗、抗武肺藥物、檢驗試劑。雖然台灣在武肺防疫堪稱世界優等生,卻也因防疫太優秀、確診數較他國少很多,導致在武肺疫苗、抗武肺藥物研發上缺乏臨床實驗樣本數,進而影響國產武肺疫苗問世時程。繼衛福部食品藥物管理署於8月17日宣布,將有條件核准國光生技研發的武肺疫苗,進入第一期臨床試驗後,食藥署今(31)日再宣布,將有條件核准高端疫苗生物製劑研發的武肺疫苗,進入第一期臨床試驗。
食藥署表示,考量COVID-19疫情緊急公共衛生情事,國內亟需治療疫苗以維護國人健康權益,於2020年8月26日召開「高端疫苗生物製劑股份有限公司(後簡稱高端公司)COVID-19疫苗第一期臨床試驗案審查專家會議」,審查其COVID-19候選疫苗「MVC-COV1901 vaccine(SARS-CoV-2 S-2P棘蛋白) Injection」之第一期臨床試驗計畫,會議決議待廠商補件並經審查同意後,得有條件核准該試驗計畫。
高端公司遂於2020年8月28日提交補件資料,並經衛福部審查通過,有條件核准其第一期臨床試驗計畫,惟疫苗是否有效仍待試驗結果進一步評估。
食藥署表示,該試驗計畫為首次用於人體之疫苗臨床試驗對受試者之安全,可能有其潛在之風險,為求審查之周延,食藥署特邀請國內藥毒理、藥物製程開發、疫苗及臨床醫學專家、學者召開會議討論,基於國內公共衛生需求、病患醫療利益與風險之整體評估,與會專家建議依據同類產品審查一致性原則,如廠商補件資料齊備並經審查同意,得有條件核准該第一期臨床試驗計畫。
食藥署也說,高端公司後續於2020年8月28日所提交之補件資料,經衛福部審查符合臨床試驗第一期安全性之法規要求,因此,有條件核准高端公司之第一期臨床試驗計畫,即要求該公司須補齊部分技術性資料,並經衛福部審查通過後,方可實際施打於受試者,以保障受試者的權益。
※台灣好新聞提醒您:武漢肺炎防疫不恐慌!
肥皂勤洗手、公共場所戴口罩,減少聚會不握手,避免接觸禽畜類動物、生食肉品!
國外入境若身體不適主動通報機場及港口檢疫人員,出現疑似症狀撥打防疫專線,戴口罩儘速就醫,並告知醫師旅遊史。
※免付費防疫專線:1922、0800-001-922











